
诺华制药业务总监Epstein在评论这一消息时称:「对于美国的强直性脊柱炎与银屑病性关节炎患者来说,这两种适应症的获批是一个潜在的转折点,因为Cosentyx提供了一种新的靶向方法,可以抑制这些疾病的炎症过程。我们研究的结果显示,大多数以Cosentyx治疗的患者其强直性脊柱炎与银屑病性关节炎体征与症状明显减轻,从事日常活动的能力显示有重大改善。」
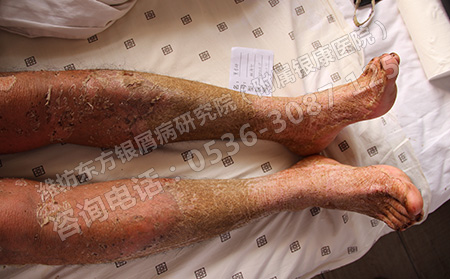
此次批准基于四项安慰剂对照3期研究的有效性与安全性结果,这四项研究包括了逾1500名活动性强直性脊柱炎或活动性银屑病性关节炎患者,他们既往未接受过生物药治疗或对抗TNFs药物没有充分响应/不耐受。
这两种适应症获批之前,FDA已批准Cosentyx用于中重度斑块状银屑病成年患者治疗,2015年11月欧洲获批该药物用于活动性强直性脊柱炎与活动性银屑病性关节炎治疗。
美国FDA批准诺华Cosentyx(secukinumab)用于活动性强直性脊柱炎(AS)及活动性银屑病性关节炎(PsA)成年患者治疗。Cosentyx是一种全人源单克隆抗体,它可选择性中和循环的白介素-17A(IL-17A)。研究表明,IL-17A在银屑病、活动性强直性脊柱炎与活动性银屑病性关节炎中,对激发人体免疫响应可起到重要的作用。
在活动性强直性脊柱炎或活动性银屑病性关节炎中,ASAS20和ACR20是用来评价临床改善的标准工具。临床试验中有9600多名患者已使用Cosentyx用于多种适应症治疗,产品上市后,有逾1.5万银屑病患者已使用该药物进行治疗。Cosentyx的安全性显示与用于多种适应症的临床试验所观察到的一致。
在研究中,Cosentyx达到了主要终点,即与安慰剂相比,Cosentyx治疗患者在活动性强直性脊柱炎与活动性银屑病性关节炎体征与症状上获得具有统计学意义的明显改善,评价指标为16周时以脊柱关节炎国际社会评估标准(ASAS20)评价,体征与症状至少有20%的改善,在24周时以美国风湿病学会响应标准(ACR20)评价,体征与症状至少有20%的减轻。